Le service de biologie moléculaire assure la mise en œuvre de techniques moléculaires pour l’analyse et la caractérisation de la biodiversité. Nous avons une longue expérience de l’utilisation d’ADN environnemental (ADNe) extrait à partir de diverses matrices environnementales (e.g. eau, sol, sédiments, fèces, pollen).
Techniques de biologie moléculaire
Les principales techniques de biologie moléculaire utilisées sur le plateau sont les suivantes :
- Extraction des acides nucléiques : ADN et ARN à partir de diverses matrices (tissus, sol, eau, bulk, …)
- Préparation de PCR pour du séquençage Sanger ou du métabarcoding
- Construction de banques pour le séquençage haut débit
- Contrôle qualité des échantillons (quantification, pureté et analyse de la taille)
- Quantification absolue par détection et quantification spécifique par dPCR
Approches
Nous mettons en pratique les méthodes suivantes :
- Métabarcoding : Identification simultanée et taxonomique d’un pool d’espèces au sein d’un échantillon complexe, basée sur le séquençage d’un marqueur (barcode) spécifique.
- Métagénomique : Caractérisation globale des communautés microbiennes présentes dans un échantillon, par le séquençage de l’intégralité de l’ADN (shotgun) pour analyser à la fois la diversité et les fonctions génétiques.
- Barcoding : Identification spécifique d’un individu ou d’une espèce unique (spécimen) grâce au séquençage d’une séquence ADN marqueur (le code-barres).
- Genome Skimming : Séquençage haut-débit de faible profondeur afin de ne garder que les zones fortement répétées. Cela nous permet par exemple de reconstruire les génomes d’organelles par exemple (mitochondrie, chloroplaste) Reconstruction rapide des génomes d’organelles (mitochondrie, chloroplaste) et récupération de séquences répétées, obtenue par séquençage shotgun à faible profondeur.
- Capture (ou Hybridation) : Enrichissement ciblé de fragments d’ADN ou d’une séquence génomique d’intérêt (target enrichment), visant à maximiser la couverture de cette cible lors du séquençage haut débit (NGS).

Le service de bioinformatique est dédié aux activités suivantes :
- Développement d’outils informatiques pour l’analyse de données biologiques
- Développement de procédures de traitement automatisé des données biologiques
- Traitement et analyse des données de séquençage ADN, en particulier des données de métabarcoding
- Assemblage de génomes par genome skimming (e.g. assemblage de mitogénomes)
- Analyse de séquençage de première génération
- Génotypage de microsatellites
- Conseil et assistance des personnels et étudiants dans l’analyse des données
- Formations régulières en informatique (systèmes Unix, clusters de calcul, R Markdown) et bioinformatique (analyse de données de métabarcoding ADN)
- Organisation de la mise en forme et du stockage de données biologiques

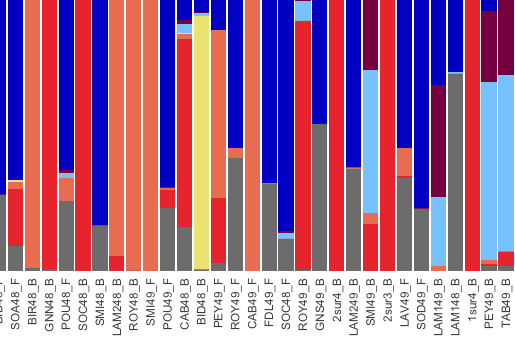
Les collections biologiques du CRBE sont au service des projets de recherche de l’unité. Elles permettent la sécurisation, la pérennisation et la gestion efficace des échantillons acquis depuis 1985 dans le cadre des multiples projets de recherche. Nous accompagnons le travail de recherche en rendant les échantillons rapidement accessibles et répondons aux contraintes de la loi 2016 pour la reconquête de la biodiversité (archivage et traçabilité des échantillons biologiques pour une période de 20 ans). Cette collection est composée de plus de 200 000 échantillons (animaux, végétaux, champignons, micro-organismes) qui incluent spécimens, tissus et ADN.
La base de données des collections biologiques est consultable ici.


Le service de Microbiologie développe et coordonne des projets de recherche autour des interactions entre les microorganismes et leurs environnements, qu’ils soient naturels ou anthropisés. Notre mission est de fournir expertise, méthodologies et outils innovants pour étudier et comprendre ces interactions, en appui aux chercheurs et partenaires scientifiques.
Domaines d’expertise
- Étude des interactions microorganismes-hôtes : Conception de protocoles expérimentaux et développement d’outils d’analyse pour explorer les relations symbiotiques, pathogènes ou mutualistes entre microorganismes et organismes hôtes.
- Microbiologie environnementale : Suivi et analyse de la diversité microbienne dans différents milieux (eaux douces, eaux usées, sols, animaux …), en intégrant des méthodes de culture, d’isolement, d’identification et de quantification.
- Biologie moléculaire appliquée au microbiote : Utilisation de techniques d’ADN/ARN, PCR digitale, metabarcoding, séquençage et analyses bioinformatiques pour caractériser les communautés microbiennes et leurs fonctions.
- Développement méthodologique : Mise au point et validation de nouvelles méthodes pour la détection et la quantification de microorganismes spécifiques.
Approches
Notre travail repose sur une combinaison de méthodes classiques et innovantes :
- Microbiologie de culture et de terrain : culture, isolement et mise en collection de bactéries et champignons
- Cinétiques bactériennes (de croissance et d’infestation) et quantifications (haut-débit, cytométrie, dPCR)
- Phénotypage à haut débit, analyses moléculaires et bioinformatiques
- Développement d’outils spécifiques (sondes, amorces, protocoles)
- Collaboration interdisciplinaire avec diverses équipes de recherche
Exemples d’applications de nos travaux
- Etude des facteurs qui influencent la dynamique des agents pathogènes dans les relations symbiotiques.
- Suivi de la qualité de l’eau et évaluation des solutions de traitement fondées sur la nature.
- Recherche de solutions biologiques de lutte contre les microorganismes pathogènes (cocultures phages/bactéries).
- Analyse de l’influence du microbiome sur la santé humaine et animale, dans différents contextes environnementaux.